鉅大LARGE | 點(diǎn)擊量:3065次 | 2018年09月29日
鋰離子電池的動(dòng)力學(xué)過程及其數(shù)學(xué)描述
從電子設(shè)備的電源,到新能源電動(dòng)汽車的動(dòng)力電源,鋰離子電池已經(jīng)深入到人類日常生活的方方面面。本文將以另一個(gè)視角帶領(lǐng)大家深入鋰離子電池內(nèi)部,去看看在鋰離子電池正常充放電過程中,其內(nèi)部發(fā)生了什么樣的物理化學(xué)現(xiàn)象,以及如何利用數(shù)學(xué)方法對這些現(xiàn)象進(jìn)行描述。
所有的物理化學(xué)過程都是以幾何結(jié)構(gòu)為載體的,本文首先介紹了鋰離子電池的幾何結(jié)構(gòu),然后以此為基礎(chǔ)介紹了鋰離子電池的動(dòng)力學(xué)過程及其數(shù)學(xué)描述。
1.鋰離子電池的“三明治”結(jié)構(gòu)
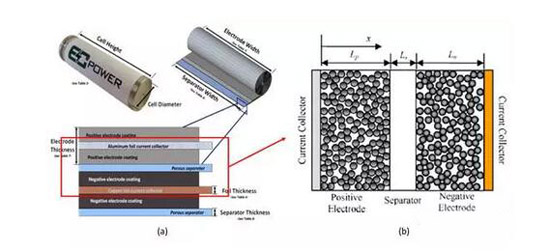
圖1鋰離子電池結(jié)構(gòu)
所有的鋰離子電池,包括不同體系(鈷酸鋰、錳酸鋰、鎳鈷錳三元和磷酸鐵鋰等)和不同制造工藝(卷繞和碟片等),其內(nèi)部都是由若干基本的單元組成的,如圖1(a)紅色方框所示。
該基本單元又可以分為5個(gè)區(qū),如圖1(b)所示,從左到右依次是:正極集流體、正極極片、隔離膜、負(fù)極極片和負(fù)極集流體。其中,正、負(fù)極集流體一般分別為鋁箔和銅箔;正、負(fù)極極片是由活性材料、導(dǎo)電材料和粘接劑等混合之后均勻涂在正、負(fù)極集流體上形成的一層多孔介質(zhì),可以通過電解液;隔離膜為允許鋰離子通過但不允許電子通過的多孔介質(zhì)。
這種基本單元的結(jié)構(gòu)在外形上與三明治極為相似,因此也將該基本單元形容成“三明治”結(jié)構(gòu)。該“三明治”結(jié)構(gòu),也是鋰離子電池所有物理化學(xué)過程的載體,接下來將以此為基礎(chǔ)對鋰離子電池的動(dòng)力學(xué)過程(物理化學(xué)過程)進(jìn)行說明。
2.鋰離子電池的動(dòng)力學(xué)過程
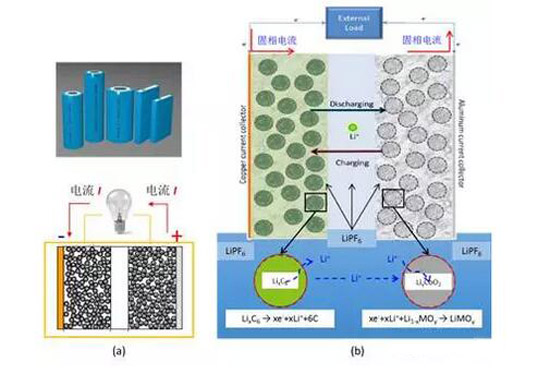
圖2鋰離子電池動(dòng)力學(xué)過程的原理圖
當(dāng)鋰離子電池接入回路(接入負(fù)載或者外部電源)中時(shí),就會(huì)出現(xiàn)一系列的物理化學(xué)變化。本節(jié)以鋰離子放電過程為例,來揭示鋰離子電池內(nèi)部的動(dòng)力學(xué)過程。充電過程與放電過程的原理是一樣的,區(qū)別只是電荷運(yùn)動(dòng)的方向相反。
圖2(a)為幾種鋰離子電池及其使用過程的示意,圖2(b)為鋰離子電池動(dòng)力學(xué)過程的原理圖。為了便于建立模型,活性材料被簡化成球形,負(fù)極用LixC6表示,正極用LiMOy表示。
如圖2(b)所示,當(dāng)鋰離子電池接入負(fù)載時(shí),電極(正、負(fù)極極片)電壓就會(huì)越過平衡電壓,開路情況下的平衡狀態(tài)被打破,負(fù)極和正極分別發(fā)生式(1)和式(2)的化學(xué)反應(yīng),
LixC6→xe-+xLi++6C式(1)
xe-+xLi++Li1-xMOy→LiMOy式(2)
這兩個(gè)化學(xué)反應(yīng)是由電流激發(fā)的,因此稱為電化學(xué)反應(yīng)。電化學(xué)反應(yīng)會(huì)使Li+(鋰離子)從負(fù)極活性顆粒中脫出,并嵌入正極活性顆粒中,這個(gè)過程稱為電化學(xué)過程。
Li+是從活性顆粒表面脫嵌的,因此活性顆粒內(nèi)部會(huì)出現(xiàn)一個(gè)Li+的濃度梯度。在這個(gè)濃度梯度的驅(qū)動(dòng)下,Li+在活性顆粒中擴(kuò)散,這個(gè)過程稱為固相擴(kuò)散過程。
當(dāng)Li+從負(fù)極活性顆粒中脫出之后,負(fù)極極片周圍的電解液中Li+濃度升高,當(dāng)Li+嵌入到正極活性顆粒之后,正極極片周圍的電解液中Li+濃度降低,這樣在電池內(nèi)部電解液中存在著濃度梯度,在這個(gè)濃度梯度的驅(qū)動(dòng)下Li+從負(fù)極擴(kuò)散到正極,同時(shí)Li+會(huì)受到電遷移和對流等因素的影響而運(yùn)動(dòng),這個(gè)過程稱為液相擴(kuò)散過程。
在集流體和極片上,存在電子的轉(zhuǎn)移以及Li+的產(chǎn)生和吸收,因此集流體和極片上電勢會(huì)出現(xiàn)變化,這個(gè)過程稱為固相電勢過程。
在電解液中,存在這Li+的擴(kuò)散、遷移、對流、產(chǎn)生和吸收,因此電解液的電勢會(huì)出現(xiàn)變化,這個(gè)過程稱為液相電勢過程。
3.動(dòng)力學(xué)過程的數(shù)學(xué)描述
清楚了鋰離子電池的動(dòng)力學(xué)過程之后,需要對其進(jìn)行數(shù)學(xué)描述,這樣才可能為實(shí)際生產(chǎn)提供指導(dǎo)。本節(jié)對就上節(jié)的5個(gè)過程進(jìn)行數(shù)學(xué)描述。
(a)電化學(xué)過程的數(shù)學(xué)描述

Li+在活性顆粒表面的脫嵌過程由式(3)來描述。其中,i1oc為電化學(xué)反應(yīng)電流密度,是Li+脫嵌過程中形成的電流,它是描述電化學(xué)反應(yīng)劇烈程度的參數(shù);i0為交換電流密度,是平衡狀態(tài)Li+脫嵌過程中形成的電流,它與溫度、Li+濃度以及化學(xué)反應(yīng)類型等有關(guān),是一個(gè)狀態(tài)參數(shù);η為過電勢,是電極電勢越過平衡電勢的值,它是電化學(xué)反應(yīng)的驅(qū)動(dòng)力。
(b)固相擴(kuò)散過程的數(shù)學(xué)描述
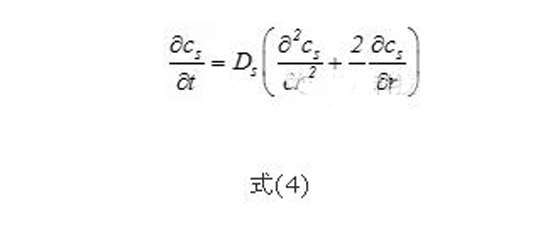
Li+在活性顆粒內(nèi)部的擴(kuò)散過程由式(4)來描述。其中,Cs為活性顆粒中Li+的濃度。該過程由濃度梯度驅(qū)動(dòng)。
(c)液相擴(kuò)散過程的數(shù)學(xué)描述
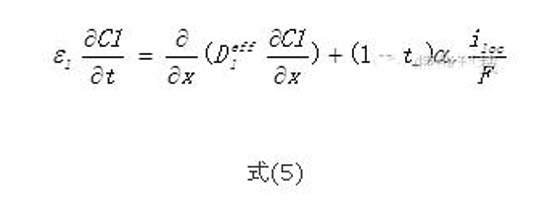
Li+在電解液中的擴(kuò)散過程由式(5)來描述。其中,C1為電解液中Li+的濃度。該過程由濃度梯度、電遷移等驅(qū)動(dòng)。
(d)固相電勢過程的數(shù)學(xué)描述
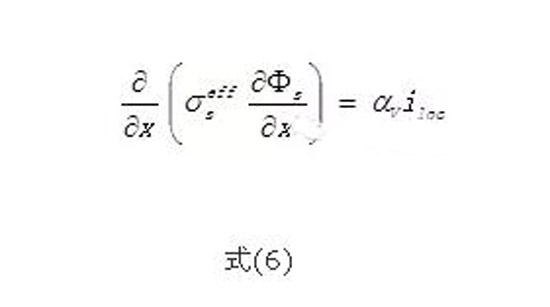
集流體和極片的電勢值可以由式(6)來計(jì)算。其中,ФS為集流體和極片的電勢值。式(6)實(shí)際上是歐姆定律的一種變形。
(e)液相電勢過程的數(shù)學(xué)描述
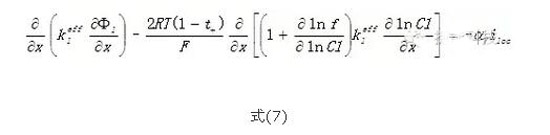
電解液的電勢值可以由式(7)來計(jì)算。其中,Ф1為電解液的電勢值。式(7)實(shí)際上也是歐姆定律的一種變形。
附錄電化學(xué)仿真實(shí)例展示
通過數(shù)學(xué)模型將鋰離子電池的充放電過程進(jìn)行描述之后,可以求解出鋰離子電池的參數(shù)。圖3所示的是通過數(shù)值模擬方法獲得的電池充放電曲線。
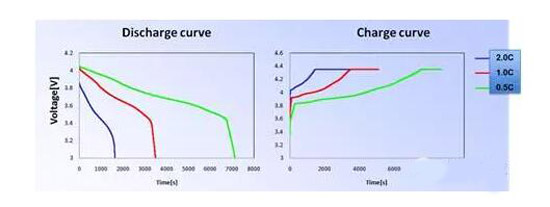
圖3電化學(xué)仿真得出的鋰離子電池充放電曲線

























